医療用IDおよびバーコードの読み取りを自動化する機器固有識別技術
DigiKeyの北米担当編集者の提供
2023-10-26
2013年、米国食品医薬品局(FDA)は機器固有識別システム(UDI)規則を導入しました。この規則は、製造、流通、使用の各段階で、最新のドキュメントを使用して医療機器の追跡と識別の一貫した方法を提供することにより、患者の安全性を向上させることを目的としています。欧州の医療機器規制要件や他国の類似した規制と同様に、米国のUDI規則はレポート精度を高め、リコールや有害事象発生時の分析を容易にします。
FDAは2023年9月24日より、機器のラベルおよびパッケージに対して米国医療関連商品コードおよび米国医薬品コード番号を含めることを完全に施行しています。この日以降にラベル付けされる医療製品は、UDI要件に完全に準拠する必要があります。この義務化は次のような製品に影響を与えます。
- ペースメーカーや埋め込み型補綴物など、クラス3の安全を最重視すべき製品
- 注射器、カテーテル、吸収性縫合糸など、クラス2の中程度に重要な製品
- デンタルフロス、医療用ガウン、酸素マスクなど、クラス1のリスクが低い製品
この義務化の完全施行は、医療機器にスキャン可能なバーコードがない場合、人間が読めるラベルがあっても、また一般的にほとんどのユーザーが容易に識別できると思われる製品であっても、有効/使用可能な製品とはみなされなくなることを意味します。この完全施行は、医療業界と医療保険請求における包括的なコード番号の採用を促進することになるでしょう。
 図1:一部のハンドヘルド型ダイレクトパーツマーク(DPM)バーコード検証機は、高度な照明や他のソフトウェアを備えており、シンボルを自動的に検出し、手元にある特定のDPMマークや材料基板の読み取り設定をサイクルして最適化します。実際、画像にあるLVS-9585は、包括的な分析とレポートのためにDPM部品と印刷されたラベルの両方を検証できます。(画像提供:Omron Automation)
図1:一部のハンドヘルド型ダイレクトパーツマーク(DPM)バーコード検証機は、高度な照明や他のソフトウェアを備えており、シンボルを自動的に検出し、手元にある特定のDPMマークや材料基板の読み取り設定をサイクルして最適化します。実際、画像にあるLVS-9585は、包括的な分析とレポートのためにDPM部品と印刷されたラベルの両方を検証できます。(画像提供:Omron Automation)
責任を負う契約企業(ブランド保持者)
米国では、全医療製品の知的財産権所有者とユーザー向けブランドが、UDIコードの精度と品質に関する責任を負います。医療製品市場の多くが受託生産で、他の企業の施設にアウトソーシングされているため、これは特に重要です。したがって、サプライチェーン全体がUDIに準拠し、正確なラベルを作成することは、契約企業の責任です。
機器固有識別技術の起源
UDIは静的な機器識別子です。しかし、パッケージ内の品目の数量変化により、新たな識別子が必要となる可能性があります。これらの詳細を区別する方法は、発行機関が決定します。同じように、機器の梱包の無菌条件を変更すると、機器識別子も変更される可能性があります。機器の販売先市場(機器が販売される国)、ラベルの言語、またはCEマークを変更する場合にも、機器識別子の変更が必要になることがあります。
UDI規則以前は、医療機器メーカーが製品に特定の品番をラベル付けしていたかもしれません。医療機関や病院が再び品番を変更する前に、ディストリビュータがその品番を変更することもありました。患者の手元に届く前に、あらゆる企業が品番を変更する可能性があり、製品の追跡、リコールへの対応、偽造の防止、新しい在庫の正確な発注を効率的に行うことはほぼ不可能でした。
現在、UDIと呼ばれる標準化された永続的識別子がすべての機器に付与され、すべての企業がより迅速かつ正確に機器を識別できるようになり、最終的には医療過誤が減少させることが可能です。このUDIは、次の2つの重要なデータを含む英数字コードです。
- 機器識別子
- 製造識別子
機器識別子は、ラベラ(通常は機器メーカー)と機器の特定のモデル番号を記載する、所定の機器に割り当てられた静的ラベルです。対照的に、製造識別子は変動可能なデータを含み、そのデータの多くはオプションです。その中にはロットコード、バッチコード、シリアル番号、有効期限、製造日を含めることができます。要するに、オプションのデータは、メーカーやラベラが機器追跡をサポートするために必要と考えるものであれば、何でも含めることが可能です。
すべてのUDIラベルは、この情報を次の2つの形式で表示する必要があります。
- 対人可読形式(プレーンテキスト)
- 機械可読形式(バーコードまたはRFIDリーダで読み取り可能)
機器が複数の医療アプリケーションに適合できる場合、UDIはその包装ではなく、機器に直接マークする必要があります。この規則は、複数回使用可能な機器にも適用されます。
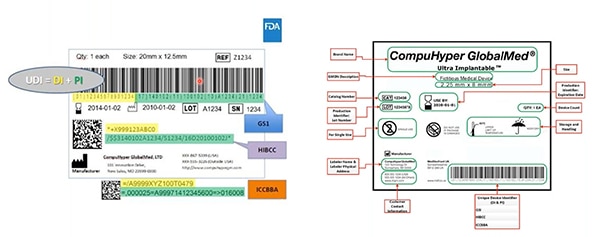 図2:UDIの発行機関であるGS1、HIBCC、ICCBBAはUDIを作成し、UDIに許容可能なシンボルを割り当て、UDIと連動する技術を定義し、UDIマークに要求される品質を規定します。このサンプルでは黄色で強調表示されているのが機器識別子、緑色で強調表示されているのが製造識別子です。その他の要素には人間が読める情報が含まれており、これは機械可読バーコードにもエンコードされています。(画像提供:FDA)
図2:UDIの発行機関であるGS1、HIBCC、ICCBBAはUDIを作成し、UDIに許容可能なシンボルを割り当て、UDIと連動する技術を定義し、UDIマークに要求される品質を規定します。このサンプルでは黄色で強調表示されているのが機器識別子、緑色で強調表示されているのが製造識別子です。その他の要素には人間が読める情報が含まれており、これは機械可読バーコードにもエンコードされています。(画像提供:FDA)
リコール時の追跡を可能にし、特定の機器に関する情報を一般に公開するため、すべての機器をグローバルUDIデータベースに登録する必要があります。FDAの認定を受けた発行機関には、機器メーカーが製品に付与する一意の識別子を作成する権限があります。
関連ホワイトペーパー:トレーサビリティに関する最新情報
UDIスキャン技術とテクニック
UDIラベルは製造から使用までの過程で、複数の方法によって検証できます。
インライン検証は、製造時に膨大な数の製品を迅速かつ正確に処理するために、大型機械に統合された技術によって実行されます。これらの技術は高度なソフトウェアに支えられており、場合によっては産業グレードのラベルプリンタが使用されます。これらのプリンタは、独自のインライン検証機能を備えています。そのため、ラベルが作成されるとすぐに、UDI情報が厳密な業界標準に従い、読み取り可能であることを確認できます。たとえば、Omron AutomationのV275検証機は、Zebraのサーマルプリンタと組み合わせて使用され、ISO 15426規格および発行機関GS1の規格に準拠します。
他にも、インライン検証には、自動化された生産ラインにおける特殊なマシンビジョンを備える側面コンベアが使用されます。このコンベアは、高速生産ラインで多品種製品のUDIラベルを極めて迅速かつ正確に検証できるバーコード読み取り機能を取り入れています。Omron AutomationのMicroHAWK製品は、この分野では優れた性能を持ち、小型化された構造とEthernet/IPおよびPROFINETを含む接続オプションによって補完された高度なセンサを備えています。
関連記事:不正表示の責任を回避する
対照的に、オフラインUDI検証は、品質を保証するためのラベルのバッチサンプリングに最も適しています。オフライン検証は、医療機器が施設を出発または到着する際のサンプル検査に採用されることが多く、流通過程の上流でオンライン検証システムを補完できます。
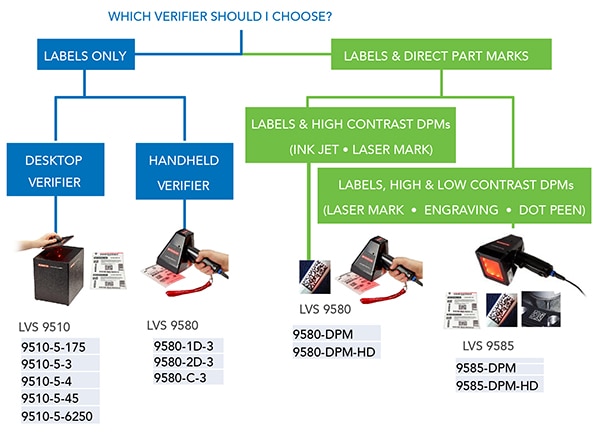 図3:製品に直接マークされたUDIは、貼付ラベルに印刷されたUDIとは異なる検証機を必要とします。(画像提供:Omron Automation)
図3:製品に直接マークされたUDIは、貼付ラベルに印刷されたUDIとは異なる検証機を必要とします。(画像提供:Omron Automation)
実際、すべての医療流通およびヘルスケア業務では、ISOに準拠した検証機を使用することで利点を得ることができます。OmronのLVS 95XXシリーズ オフラインUDI検証製品について考えてみましょう。この製品には以下が採用されています。
- コードを作成するレーザーマーキングステーションやラベルプリンタ
- 製品にコードを適用するエリア(コードの作成エリアとは別の場合もあれば、そうでない場合もあります)
- テンプレート、形式、その他のコード要素を確認する品質管理ステーション
オフラインUDI検証機のバリエーションの指定
特定のアプリケーションに最も適したオフラインUDI検証機というのは、いくつかのパラメータに依存します。
バーコードのサイズ:多くの場合、大きなバーコードは、レンズの焦点距離とセンササイズによって定義される大きな視野を持つ識別子を使用したほうがスキャンは簡単です。Omron AutomationのLVS-9510デスクトップUDI識別子について考えてみましょう。このシリーズの製品は、直線ラベルと2次元ラベルの両方を読み取ることができます。5つの異なるバージョンはそれぞれ視野が異なるため、設計者は検証する必要があるバーコードのサイズに適合するバージョンを選択できます。スティッチング機能により、視野を超えるバーコードのグレード付けが可能です。
さらに、LVS-9510の全製品は、コードの評価に必要なシンボルとアパーチャを自動的に決定し、問題箇所を特定して強調表示できます。
 図4:ISO規格を満たすバーコード検証は、直線(1D)コードと2次元(2D)コードの両方を検証できる装置によって簡単に行えます。このような装置の一部は、コードの評価に必要なシンボルとアパーチャを決定し、問題を特定して強調表示します。画像にあるLVS-9510は、視野より大きなバーコードのグレード付けを可能にするスティッチング機能を備えています。(画像提供:Omron Automation)
図4:ISO規格を満たすバーコード検証は、直線(1D)コードと2次元(2D)コードの両方を検証できる装置によって簡単に行えます。このような装置の一部は、コードの評価に必要なシンボルとアパーチャを決定し、問題を特定して強調表示します。画像にあるLVS-9510は、視野より大きなバーコードのグレード付けを可能にするスティッチング機能を備えています。(画像提供:Omron Automation)
バーコードの種類:スキャナは、HIBCC、ICCBBA、または(2023年現在最も一般的な)GS1として知られる発行機関によって割り当てられたバーコード形式を読み取る必要があります。GS1は、UPC、直線バーコード、2Dデータマトリクスバーコードの各サイズ、形式、解像度を規定しています。
UDIマークの位置:医療機器のダイレクトパーツマーキング(DPM)について考えてみましょう。これらのマークは、特に手術器具や埋め込み可能な医療機器を識別する場合、信じられないほど小さくなります。このようなDPMのUDIを読み取って検証するために、Omronの超高密度ハンドヘルド検証機LVS-9580およびLVS-9585は、セルサイズが0.002インチのものを含む、多種多様なDPMのグレード検証を行える特殊レンズを備えています。LVS-9580およびLVS-9585内の産業グレードレンズは、一貫した読み取り精度を保証します。最も洗練されているのはスキャナ内部の照明技術で、これは精密な制御と較正が可能です。複数の視野とともに、照明によりキャプチャしたUDI画像を即座に最適化できます。コード規格では事後の修正や画像操作ができないため、これは特に重要です。
UDIスキャナソフトウェアの詳細
検証機ハードウェアをサポートするUDIソフトウェアは、最大限の効果を得るために、診断情報を直感的な形式で提示する必要があります。このソフトウェアは、ISOで定義されたパラメータに従ってUDIコードをグレード付けし(最も重要なのは可読性の確認)、理想的には一連のUDIスキャンにわたって悪化する問題を追跡する必要もあります。
Omronは提供するすべてのUDIスキャンハードウェアでは、必要なソフトウェアを同梱しています。このソフトウェアは、急速に進化する規制や新しい業界法規に対応するため、定期的に更新されます。
Omronのスキャナソフトウェアの主な機能は、コード構文の処理です。要するに、すべてのバーコードや2次元コードは、製品のタイプ、ロット番号、該当する数量、有効期限、出荷情報など、関連するすべての情報を正確に抽出する必要があります。結果として得られるデータ文字列は、進化する要件、方法、医療製品の出荷先に対応するために、特定の方法で形式化する必要があります。
スキャナメーカーがソフトウェアを定期的に更新することで、エンドユーザーは新しいコードがリリースされても常に最新の状態を維持できます。
まとめ
米軍はかつて、医療業界のUDIシステムのようなUID(一意の識別子)による製品追跡システムの完全採用を目指していました。その目的は、完成したRaytheonの兵器から、特殊用途向けに小さな会社から供給された制御盤まで、あらゆるものを含む軍事施設での物資の紛失、重複、未計数に伴う膨大な無駄を抑制することでした。今日、UIDはさまざまなレベルで使用されています。
UDIの義務化は、かつてのUIDシステム導入とは異なる運命を辿るでしょう。
UDI採用を推進する合言葉は単純明快で、ラベルは製品そのものです。結局のところ、不正確なラベルは医療スタッフの時間を浪費し、医療機器の廃棄につながる一連の事態を引き起こす可能性があります。したがって、UDIは、ユニット、パッケージ、バンドル、ケース、パレットなど、包装のすべての層に表示する必要があります。滅菌シールの内側にある無菌医療機器のUDIは特に重要です。なぜなら、機器の種類を確認するためにそのシールを破ることは許されないためです。
FDAが2023年9月24日からUDI指令の完全遵守を要求する中、医療製品を検証するための高度なスキャン技術は、オートメーションメーカーだけでなく、オートメーションメーカーがサービスを提供する機械メーカーやエンドユーザーにとっても最重要となります。
そのようなスキャナは、幅広い実験機器、医療機器、臨床診断機器のラベルを確認するための、極めて厳密なFDAのUDI要件を満たすことができます。オフラインバーコード検証機はインラインマシンビジョンと高度なDPMリーダを活用し、トレーサビリティを最大化します。

免責条項:このウェブサイト上で、さまざまな著者および/またはフォーラム参加者によって表明された意見、信念や視点は、DigiKeyの意見、信念および視点またはDigiKeyの公式な方針を必ずしも反映するものではありません。




